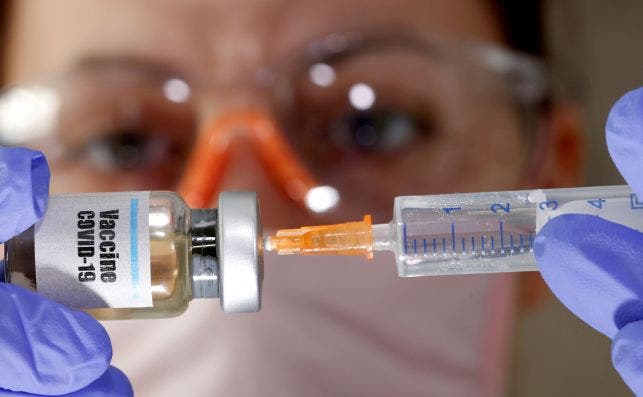
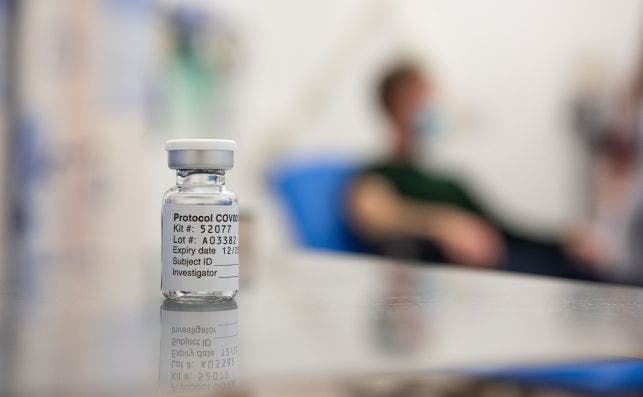
La vacuna de Oxford y Astrazeneca no convence a los EE.UU.: estos son los motivos
Oxford y Astrazeneca publican los datos completos de su vacuna en la revista 'The Lancet' para mitigar las dudas sobre su ensayo, especialmente en los EE.UU
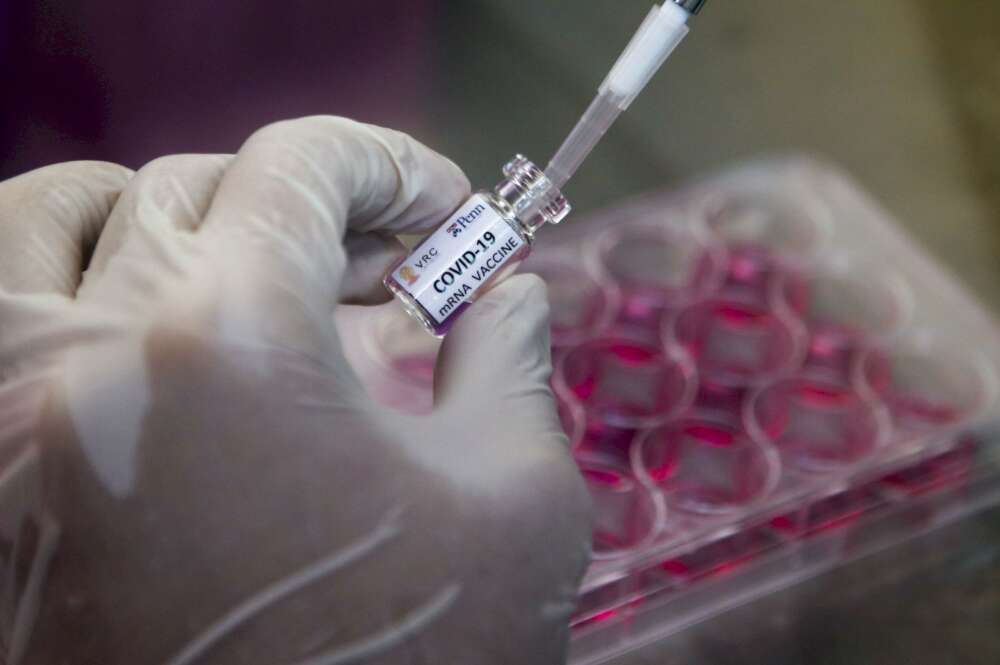
De las tres farmacéuticas que han liderado la carrera por la vacuna –Moderna, Pfizer y Astrazenca, asociada con la Universidad de Oxford-, la británica se ha quedado atrás. Varios tropezones sufridos en el sprint final han hecho que su ensayo se convierta en objeto de crítica para los medios estadounidenses. Y es que, desde que las pruebas se paralizaron en septiembre después de que una voluntaria sufriera una reacción adversa, los Estados Unidos sentenciaron esta investigación.
En un intento de volver a ganarse la confianza de las agencias reguladoras, los científicos británicos publicaron este miércoles los datos completos de su investigación en la revista médica The Lancet. “No se trata de influir en el regulador de ninguna manera, forma o forma. El regulador tomará su propia decisión basándose en todos los datos que les proporcionemos”, explicó Menelas Pangalos, vicepresidente ejecutivo de I+D de biofarmacéuticos de AstraZeneca.
«No se trata de influir en el regulador de ninguna manera, forma o forma. El regulador (estadounidense) tomará su propia decisión»
“Creo que obviamente hay muchos comentarios en los medios y en la prensa sobre la necesidad de transparencia y compartir datos”, se justificó en declaraciones recogidas por The Guardian. “Y, por supuesto, la mejor manera de hacerlo, desde una perspectiva científica, es publicar sus datos en revistas revisadas por pares de alta calidad”, añadió.
Estos son los motivos por los que será difícil que la Administración de Medicamentos y Alimentos de los Estados Unidos (FDA, por sus siglas en inglés), apruebe el antídoto inglés contra el coronavirus:
Dudas con la eficacia
Mientras que las vacunas de Moderna y Pfizer demostraron tener una eficacia superior al 95%, la de Oxford obtuvo una tasa del 70% que, aunque se encuentra dentro de los estándares inmunidad homologables exigidos, está muy por debajo. Pero tan solo unos días después de comunicar su rendimiento, las entidades británicas anunciaron una fórmula de aplicación podría aumentar su efectividad hasta el 90%.
Los fabricantes de la vacuna británica descubrieron que una primera dosis fuerte podría rebajar la eficacia de la segunda. Es decir, dos dosis completas mostraron una eficacia del 62% mientras que media dosis y, posteriormente, una entera, alcanzaba ese 90%. Uno de los principales investigadores de Oxford, Adrian Hill, explicó que «probablemente se necesitarían semanas y meses» para comprender por qué la dosis más baja producía resultados mucho mejores.
Esta explicación de la Universidad de Oxford no gustó al director del programa de vacunas estadounidense Operation Warp Speed, Moncef Slaoui, quien aseveró que el mayor nivel de efectividad se ha probado únicamente en la población joven.
De hecho, las entidades británicas anunciaron que realizarían realizarán una prueba más en el ensayo de los Estados Unidos para aclarar la incertidumbre que se ha generado en torno a la eficacia de su vacuna. Sin embargo, según el diario inglés, Astrazeneca ha concluido que no es una buena idea alterar la investigación.
Efectos adversos
El ensayo clínico de Oxford y Astrazeneca se paralizó en septiembre después de que una participante desarrollara mielitis transversa tras recibir el pinchazo, un trastorno neurológico que causa inflamación de la médula espinal.
Respecto a este acontecimiento, esta semana The New York Times criticó a Astrazeneca y Oxford por no haber informado en su momento a la FDA de que el ensayo en el Reino Unido se paralizara. El regulador estadounidense descubrió la noticia cuando Stat News la sacó a la luz, pero no recibió ningún comunicado en un primer momento.
Frente a la actitud del Reino Unido, que reanudó las pruebas poco después de sufrir el contratiempo, la agencia estadounidense esperó hasta el 23 de octubre para autorizar que continuaran las investigaciones. Esto supuso un retraso de hasta siete semanas y, en vez de reclutar a los 30.000 voluntarios previstos, tan solo consiguieron 18.000.
Menos participantes
Además, los datos de eficacia reportados por Astrazeneca se refieren a menos personas que en el caso de las otras vacunas: hasta ahora 11.636 en el Reino Unido y Brasil.
Sin embargo, hay más por venir, incluida la prueba de en los Estados Unidos financiada en parte por la Operación Warp Speed, la iniciativa para acelerar el desarrollo de la vacuna que, pese a no confiar en el antídoto inglés ha contribuido con la financiación y ordenó 300 millones de dosis.